pH et équilibre acido-basique : petite curiosité (Q1)
2 participants
Page 1 sur 1
 pH et équilibre acido-basique : petite curiosité (Q1)
pH et équilibre acido-basique : petite curiosité (Q1)
Dans le cours,
dans les tampons du LEC, on a dit que le pK pour les phosphates était de 6,8 et qu'il était moins efficace que celui des bicarbonates.
Ma question est la suivante : quel est le pK des bicarbonates ?
Supérieur à 6,8, d'accord. Mais il est de combien exactement pour avoir un ordre d'idée.
dans les tampons du LEC, on a dit que le pK pour les phosphates était de 6,8 et qu'il était moins efficace que celui des bicarbonates.
Ma question est la suivante : quel est le pK des bicarbonates ?
Supérieur à 6,8, d'accord. Mais il est de combien exactement pour avoir un ordre d'idée.
grynchou- Messages : 13
Date d'inscription : 24/01/2010
 Re: pH et équilibre acido-basique : petite curiosité (Q1)
Re: pH et équilibre acido-basique : petite curiosité (Q1)
pKa pour le couple bicarbonate/carbonate HCO3-/CO32- = 10,3
et pKa pour le couple acide carbonique/bicarbonate H2CO3/ HCO3- = 6,4
Prof physio
et pKa pour le couple acide carbonique/bicarbonate H2CO3/ HCO3- = 6,4
Prof physio
 suite de la Q1
suite de la Q1
Donc si je comprend bien (vous me stoppez si j'ai faux mais),
le couple-tampon dont on parle dans le cours est le couple bicarbonate/carbonate (pK=10,3) puisque celui-ci est plus efficace que le couple-tampon du phosphate (pK=6,
et non le couple acide carbonique/bicarbonate (pK=6,4), qui est lui, moins efficace que le couple-tampon du phosphate.
le couple-tampon dont on parle dans le cours est le couple bicarbonate/carbonate (pK=10,3) puisque celui-ci est plus efficace que le couple-tampon du phosphate (pK=6,
et non le couple acide carbonique/bicarbonate (pK=6,4), qui est lui, moins efficace que le couple-tampon du phosphate.
grynchou- Messages : 13
Date d'inscription : 24/01/2010
 Re: pH et équilibre acido-basique : petite curiosité (Q1)
Re: pH et équilibre acido-basique : petite curiosité (Q1)
Non ! Son pK est trop élevé et le carbonate n'est présent qu'en quantités homéopathiques dans le milieu intérieur dont le pH est voisin de 7,4 ! Pour vous en convaincre, tracez la courbe de dissociation de ce couple en la superposant à celle du couple acide carbonique/bicarbonate (rappelez-vous que j'ai donné en cours la similitude fonctionnelle entre CO2 et H2CO3) : je l'ai même fait pour vous ->
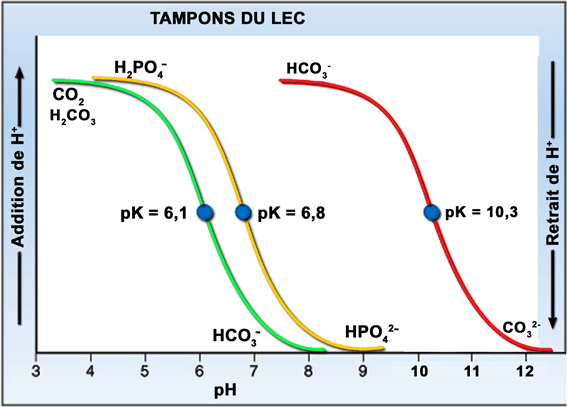
Le seul couple d'intérêt en physiologie est H2CO3/ HCO3-, le seul que j'aie mentionné à plusieurs reprises en cours : acide carbonique <-> bicarbonate. Par ailleurs, l'anhydrase carbonique ne sait pas prendre en charge le carbonate.
Prof physio

Le seul couple d'intérêt en physiologie est H2CO3/ HCO3-, le seul que j'aie mentionné à plusieurs reprises en cours : acide carbonique <-> bicarbonate. Par ailleurs, l'anhydrase carbonique ne sait pas prendre en charge le carbonate.
Prof physio
 Sujets similaires
Sujets similaires» Partie II PH et equilibre acido-basique
» Désordres acido basique
» petite question sur le Nerf
» Sur les pH et equilibres acido-basiques
» Sur l'équilibre hydrique
» Désordres acido basique
» petite question sur le Nerf
» Sur les pH et equilibres acido-basiques
» Sur l'équilibre hydrique
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|